希少疾患とは何ですか?
希少疾患について、単一かつ広く受け入れられている定義は存在しない。たとえば、世界保健機関(WHO)によると、「国際分類疾患11(ICD-11)には、約5500の希少疾患とその同義語が含まれている」(1)。米国によると食品医薬品協会(FDA)は、「7,000件以上の希少疾患が米国で3000万人以上に影響を及ぼしている」(2)。また、地域差も存在する。たとえば、米国では希少疾患は「20万人未満に影響を与える病気または状態」と定義されている(3)。ヨーロッパでは「1万人に5人未満」(4人5人)、日本では「5万人未満、つまり2500人に1人の割合」という数字である。
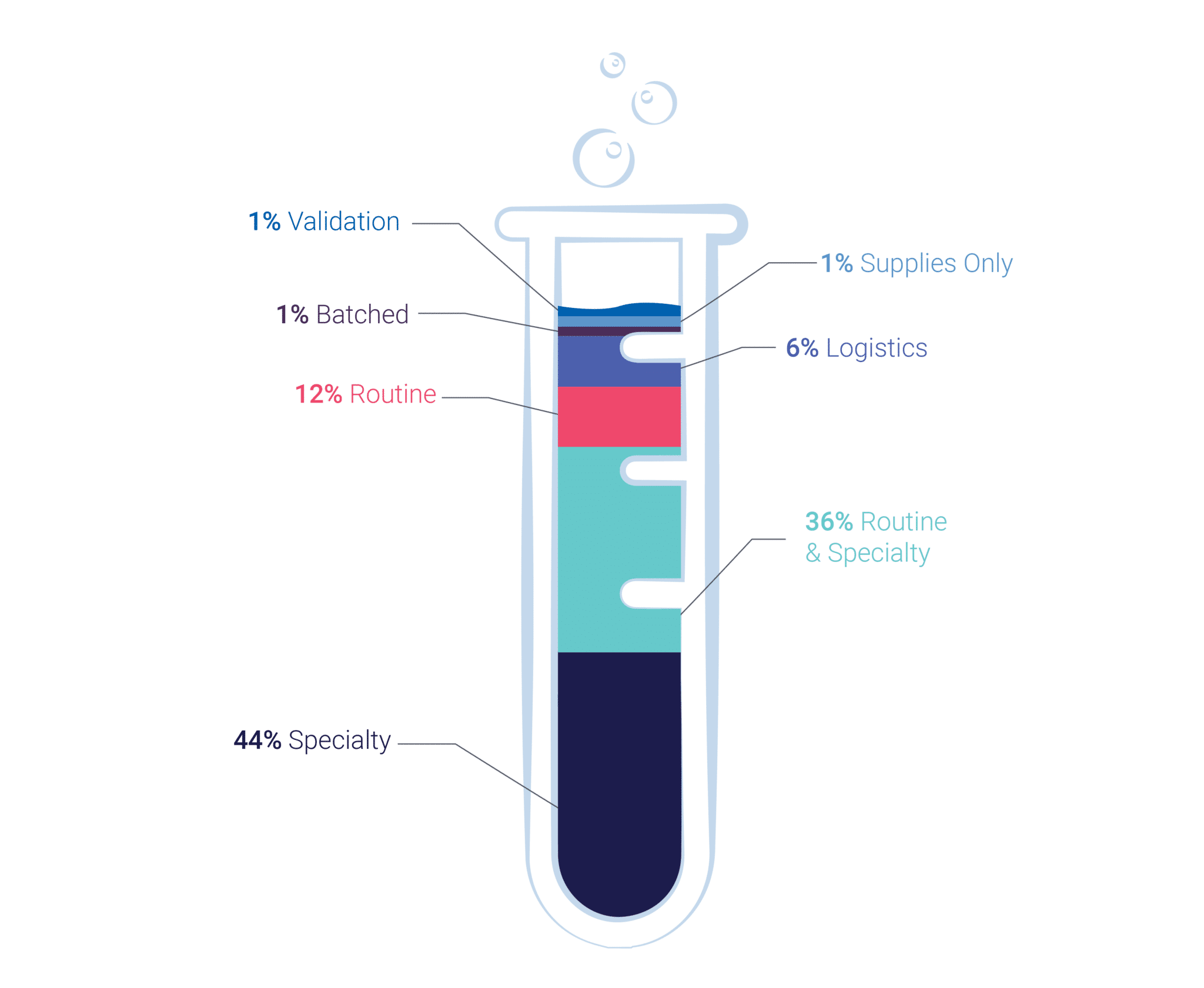
希少疾患療法の開発には、適切な患者を適切な治療および/または臨床試験に適切なタイミングで届けるために、専門知識、知識、データ、および知見へのアクセスをさらに高める必要がある。specialized logistics最先端の技術、専門分野の専門知識、専門的な物流、および業務を支援し、希少疾患の研究開発を加速します。